Metabolizam šećera u organizmu
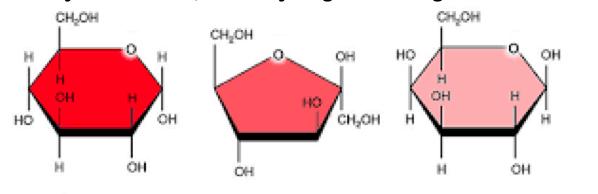
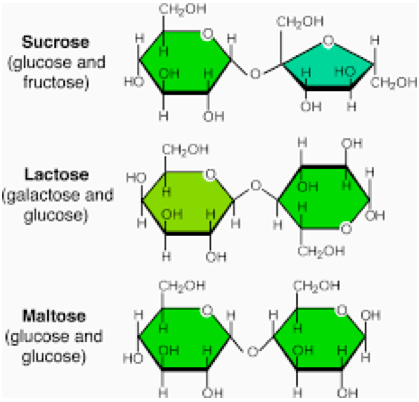
Prehrambeni šećeri koje unosimo u svoje telo mogu biti prirodnog ili industrijskog porekla. U prirodi ovi šećeri ulaze u sastav mnogih bijnih plodova, pogotovo kod voćnih biljaka, ali i kod različitih žitarica. Dobijanje šećera industrijskim putem podrazumeva upotrebu šećerne repe, šećerne trske ili kukuruza, gde finalni proizvod ovih procesa jesu saharoza ili fruktozni sirup (Sun i Empie 2012).
Sam unos ugljenih hidrata u naš organizam sa biohemijskog aspekta podrazumeva razgradnju polisaharida i disaharida na monosharide. Varenje, odnosno razgradnja ugljenih hidrata počinje u usnoj duplji, gde pljuvačna amilaza razgrađuje skrob na glukozu i maltozu. Za aktivaciju pljuvačne amilaze neophodno je prisustvo Cl- jona, kao i da pH sredine bude blago kisela (6.7). Prilikom prelaska iz usne duplje u želudac, želudačna kiselina zbog svoje niske pH vrednosti denaturiše pljuvačne amilaze i takođe razgrađuje glikozidne veze kod saharoze, pri čemu nastaju glukoza i fruktoza. Nakon spuštanja iz želuca u duodenum, iz pankreasa se oslobađaju pankreatične amilaze koje preostale molekule skroba razgrađuju na maltozu i oligosaharide. Međutim, najveći deo varenja ugljenih hidrata se dešava u tankom crevu, zato što se uneta hrana najduže zadržava tamo. Disaharide razgrađuju enzimi disaharidaze koje se nalaze u epitelnim ćelijama tankog creva.
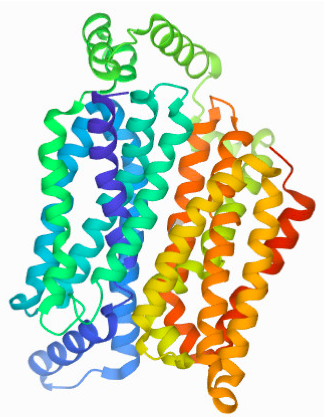
Nakon razgradnje disaharida, nastali monosaharidi se transportuju u različita tkiva kao osnovni supstrat za dobijanje ATP-a (Han i sar. 2016). Najveći deo monosaharida odlazi u hepatocite preko i ulazi u njih pomoću transportnog proteina GLUT2 koji se nalazi na membrani ovih ćelija i pripada klasi GLUT proteina (Slika 4) (Adeva-Andany i sar. 2016). U hepatocitim glukoza podleže procesu fosforilacije (koji katalizuje heksokinaza) u kojem nastaje glukoza-6-fosfat. Nastali glukoza-6-fosfat može da učestvuje u tri metabolička procesa: izomerizaciji u glukoza-1-fosfat pomoću fosfoglukomutaze, izomerizaciji u fruktoza-6-fosfat i oksidaciju u glukonolakton (Slika 5). Glukoza-1-fosfat se transformiše u UDP-glukozu koja je prekursor za sintezu glikogena, fruktoza-6-fosfat može da učestvuje u glikolizi, pri čemu kasnije nastaje piruvat, dok glukonolakton podleže pentozofosfatnom putu (Adeva-Andany i sar. 2016).
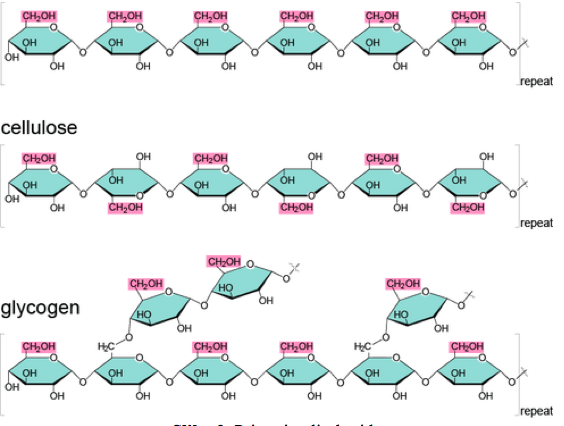
Glukoza-1-fosfat nastala izomerizacijom glukoza-6-fosfata podleže enzimskoj aktivnosti UDP-glukoza pirofosforilazi pri čemu nastaje UDP-glukoza, koja služi kao donor molekula glukoze sa sintezu glikogena (Adeva-Andany i sar. 2016). Enzim glikogenin započinje reakciju sinteze glikogena tako što se formira prvobitni lanac od 10-20 molekula glukoze. Kasnije, dalju sintezu glikogena katalizuje glikogen sintaza koja vezuje nove molekule glukoze na rastući lanac (Adeva-Andany i sar. 2016). Takođe, u ovaj proces je uključen i enzim koji potpomaže grananje molekula glikogena. Vredi napomenuti da je u toku glikogeneze inhibiran enzim glikogen fosforilaza, koji ima ključnu ulogu u procesu razgradnje glikogena (Han i sar. 2016).
Proces razgradnje glikogena podrazumeva raskidanje veza između molekula glukoze, pri čemu od jednog molekula glukoze nastaje glukoza-1-fosfat, koja može biti izomerizovana u glukozu-6-fosfat ili defosforilovana pomoću glukoza-6-fosfataze u zavisnosti od stanja u kom se organizam nalazi (Han i sar. 2016).
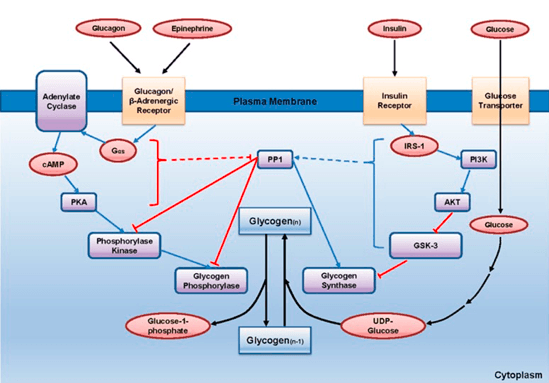
Sam promet glukoze u organizmu je pod kontrolom dva hormona: insulinom i glukagonom (Slika 6). Vezivanjem insulina za adekvatni receptor na membrani se aktivira proces unosa glukoze u ćelije, dok vezivanjem glukagon počinje kaskada kinaznih aktivnosti koje dovode do glikogenolize (Han i sar. 2016).
Kao što je napomenuto, u zavisnosti od metaboličkog stanja ćelije, izvesna količina glukoze može biti fosforilovana u glukozu-6-fosfat koja podleže procesu izomerizacije u fruktozu-6-fosfat. Fosforilovana fruktoza može da se podvrgne heksozaminskom putu ili glikolizi, pri čemu nastaje piruvat, pa kasnije acetil-CoA, koji može da uđe u Krebsov ciklus ili da učestvuje u sintezi masnih kiselina. Na sudbinu fruktoze-6-fosfata utiče i količina unetih ugljenih hidrata i ako je prevaziđen kapacitet metabolisanja uglenih hidrata, onda izvesna količina ugljenih hidrata prelazi u masti u jetri (Adeva-Andany i sar. 2016). U hepatocitima acetil-CoA napušta mitohodnrije posredstvom karnitin acetiltransferaze i tako nastaje acetil-karnitin, koji omogućuje ulazak acetilne grupe u citoplazmu (Adeva-Andany i sar. 2016). Nakon napuštanja mitohondrije, acetil-CoA karboksilaza katalizuje karboksilaciju pomenutog supstrata i tada nastaje malonil-CoA. Acetil-CoA i malonil-CoA služe za kasniju sintezu masnih kiselina, koje učestvuju u procesu lipogeneze.
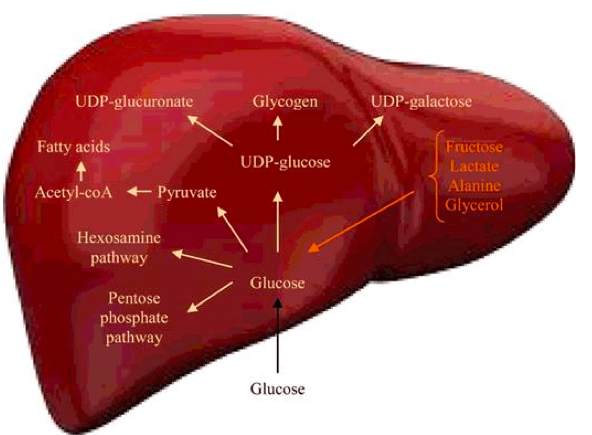
Osim kataboličkih procesa, u organizmu, tačnije jetri (Slika 7), se dešavaju i anabolički procesi (procesi sinteze) šećera i jedan od najpoznatijih primera jeste glukoneogeneza, koja kao polazna jedinjenja koristi fruktozu, laktat, alanin, glicerol (Adeva-Andany i sar. 2016). Da bi nastao molekul glukoze, neophodno je da laktat ili alanin pređu u piruvat (pomoću laktat dehidrogenaze ili alanin aminotransferaze, respektivno). Novonastali piruvat podleže karboksilaciji, pri čemu nastaje oksaloacetat, koji je supstrat u narednoj reakciji u kojoj nastaje fosfoenolpiruvat. Od fosfoenolpiruvata mogu nastati 2- ili 3-fosfoglicerat, 1,3-bisfosfoglicerat, kao i gliceraldehid 3-fosfat (Adeva-Andany i sar. 2016). U reakciji gliceraldehid 3-fosfata i dihidroksiaceton fosfata nastaje fruktoza 1,6-bisfosfat, koji prelazi u fruktozu-6-fosfat. Izomerizacijom fosforilovane fruktoze nastaje glukoza-6-fosfat.
Osim u jetri, šećeri poput glukoze imaju važnu ulogu i u mozgu, gde predstavljaju osnovni energetski supstrat i neophodni su za funkcionisanje mozga (Kleinridders i sar. 2018). Utvrđeno je da 20% od ukupne količine glukoze ide u mozak i omogućava normalno funkcionisanje mozga. Takođe je ustanovljeno da dijabetičari kod kojih se dešavaju periodične pojave hiper- i hipoglikemije imaju učestale poremećaje u radu mozga (Kleinridders i sar. 2018).
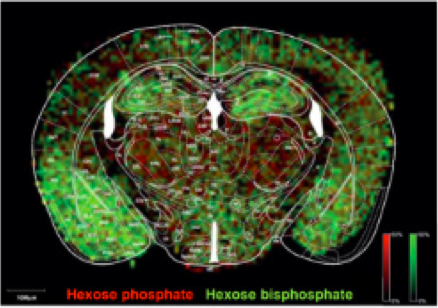
Ispitivanjem metaboličkog puta glukoze u različitim delovima mozga, ustanovljeno je da u talamusu je dominantan pentozofosfatni put, dok je glikoliza bila zastupljena u korteksu i amigdali. Ovi rezultati pokazuju da se u amigdali dešava veća isporuka glukoze u odnosu na druge regione mozga, kao i da se potvrđuje hipoteza da molekuli glukoze, koji su dostupni u ćelijama talamusa, se podvrgavaju reakcijama pentozofosfatnog puta (Kleinridders i sar. 2018).
Za sam kraj ove složene teme, treba napomenuti da šećeri imaju krucijalnu ulogu u ishrani i da predstavljaju važan izvor energije. Uz ovaj podatak se treba pozivati na činjenicu da u slučaju viška unetih šećera, dolazi do preusmeravanja metabolizma šećera radi stvaranja masti, što dovodi do gojaznosti i kasnijih zdravstvenih problema. Brinite se o sebi i hranite se odgovorno!
Literatura
Adeva-Andany MM, Peréz-Felpete N, Fernández CF et al, 2016, Liver glucose metabolism in humans, Biosci Rep, 36 (6): e00416
Han HS, Kang G, Kim JS et al, 2016, Regulation of glucose metabolism from a liver-centric perspective, Exp Mol Med, 48 (3): e218
Kleinridders A, Ferris HA, Reyzer ML et al. 2018, Regional differences in brain glucose metabolism determined by imaging mass spectrometry, Mol Metab, 12: 113-121
Sun SZ, Empie MW, 2012, Fructose metabolism in humans – what isotopic tracer studies tell us, Nutr Metab 9: 89