LIJEČENJE DIJABETESA STEM ĆELIJAMA
Matične ćelije su ćelije koštane srži koje imaju niz osobina uključujući sposobnost samoobnavljanja, diferencijacije i proliferacije. Zahvaljujući ovoj mogućnosti, stem ćelije mogu stvarati različite vrste tkiva u našem organizmu i diferencirati se u bilo koji tip ćelije. One mogu ''popravljati'' organe i tkiva oštećene nekim patološkim procesom i na taj način obnoviti taj dio organizma. Veoma su slični malim limfocitima i ima ih od 100 hiljada do milion. Dijele se svakih 5 dana, sa ukupno 300 do 500 mitoza u životu što im daje ograničen period obavljanja tako da samim time, i umiru vremenom.
Postoje 3 oblika matičnih ćelija:
1. Embrionalne matične ćelije, porijeklom od blastociste
2. Odrasle matične ćelije, u tkivima odraslog čovjeka
3. Rebraste matične ćelije, u rebrima
Porijeklo matičnih ćelija:
Kako bi imale sposobnost samoobavljanja i diferencijacije, matične ćelije prolaze kroz 2 tipa dioba:
1. Simetrična dioba
2. Asimetrična dioba
Kod ljudi postoje tri dostupna izvora autolognih stem ćelija: koštana srž, masno tkivo i krv. Matične ćelije se također mogu prikupiti iz krvi pupčane vrpce odmah nakon rađanja. Adultne matične ćelije se često koriste.
Diabetes melitus (DM), u svim svojim oblicima, je metabolički poremećaj koji nastaje zbog manjka proizvodnje inzulina u gušterači. Fiziološka kontrola razine glukoze u krvi može se obnoviti na više načina: egzogena primjena inzulina, lijekovi koji stimuliraju inzulin, lijekovi koji smanjuju inzulinsku rezistenciju i/ili zamjenjuju β ćelijsku masu (proizvođači inzulina). Regeneracija gušterače izgubljene funkcionalne β stanične mase je atraktivna strategija za oporavak od bolesti. Trenutni pristupi koji se koriste za zamjenu oštećenih β stanica gušterače uključuju transplantaciju Langerhansovih otočića, indukciju endogene regeneracije i primjenu β stanica dobivenih iz matičnih ćelija. Transplantacija Langerhansovih otočića gušterače pokazala se uspješnom za funkcionalnu nadoknadu oštećenih otočića. Međutim, da bi se postigla trajna metabolička kontrola tokom jedne godine, potrebno je transplantirati najmanje 2 milijuna β ćelija po kg tjelesne težine rezultira ograničenom dostupnošću zdravih otočića za ovu primjenu.
Povećana stopa uspješnosti dobivanja β-ćelija koje reagiraju na glukozu iz ljudskih matičnih ćelija potaknula je novu eru nadomjesne terapije β ćelija budući da bi terapija matičnim ćelijama potencijalno mogla isporučiti 100-200 milijuna β ćelija po transplantatu.
U svijetu je više od 415 milijuna oboljelo od dijabetesa.
Postoje tri oblika DM:
Diabetes mellitus-tip 1- Može se javiti u bilo kojem periodu života, obično je to period od djetinstva do 30 godine života. Također ovaj tip je jako rjeđi u odnosu na tip 2. Javlja se kada se se proizvodnja inzulina smanji na minimum. Najčešći razlog nastanka dijabetesa tip 1 je aktivacija imunološkog odgovora koji dovodi do potpunog uništenja beta ćelija Langerhansovih otočića gušterače, a zbog brzine se nastanka i dijagnoza postavlja vrlo brzo.
Diabetes mellitus tip 2- Obično se javlja u dobi poslije 40 godina. Pretilost je vrlo učestala kod osoba sa šećernom bolesti tipa 2, tako da čak i umjereni dobitak težine može povećati podložnost obolijevanja od šećerne bolesti. Masno tkivo oko abdomena i na gornjem dijelu tijela (oblik jabuke) dovodi se u vezu s inzulinskom rezistencijom , srčanom bolešću, visokim krvnim pritiskom, moždanim udarom i povišenim holesterolom.
Gestacijski tip- javlja se kod trudnica. Obično ne zahtjeva terapiju, dovoljna je regulacija ishrane te povećana fizička aktivnost.
Primjena ili injekcija egzogenog inzulina ne može zamijeniti endogeni inzulin koji luči zdrava gušterača. Mogućnost liječenja DM jeste trasplantacija gušterače. Ono što predstavlja poteškoću u takvom obliku liječenja jest ograničen broj mogućih donora gušterače, kao i doživotna potreba za imunosupresivnom terapijom kojoj je svrha spriječiti odbacivanje transplantiranog organa.
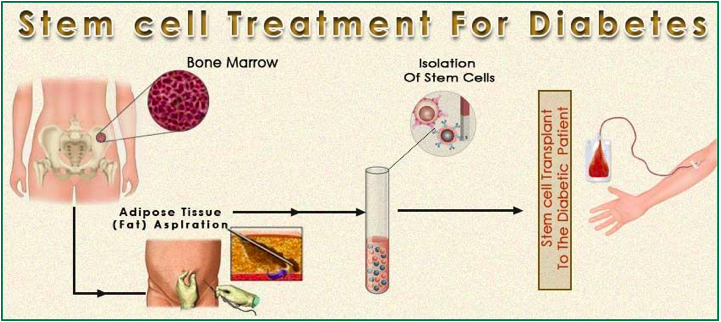
Slika 1. Liječenje dijabetesa stem ćelijama
Sa pojavom istraživanja o terapiji matičnim ćelijama za različite bolesti, zabilježena su otkrića u terapiji T1DM zasnovanoj na matičnim ćelijama. Prvi eksperiment urađen je 1980-tih godina na eksperimantalnim životnjama, a 2000. godine na čovjeku. Idealan tretman za dijabetes trebao bi obnoviti proizvodnju inzulina i regulaciju lučenja inzulina.

Slika 2. Načini liječenja dijabetesa tipa 1
ESC su pluripotentne ćelije izolovane iz unutrašnje ćelijske mase blastociste, ranog embriona sisara koji se implantira u matericu. ESC pokazuju karakteristike beskonačnog proliferativnog kapaciteta i samoobnavljanja i sposobni su da se diferenciraju u više tipova odraslih ćelija in vitro. iPSC (insulin producing cells) , koji se reprogramiraju iz somatskih ćelija, imaju sličan kapacitet da se razmnožavaju i diferenciraju kao ESC. Stoga, hPSC-i pružaju obećavajuću platformu za proizvodnju in vitro ćelija koje luče inzulin. Etička pitanja u primjeni ESC-a su još uvijek kontroverzna zbog njihovog porijekla. Nasuprot tome, iPSC su izvedeni iz odraslih somatskih ćelija koje su reprogramirane nazad u pluripotentno stanje nalik embrionu koristeći Yamanaka faktore . Tokom posljednje dvije decenije, zabilježene su brojne metode za generiranje IPC-a iz hPSC-a.
Obično su šeme za generisanje funkcionalnih IPC-a iz hPSC-a bile zasnovane na imitaciji in vivo razvoja embrionalnog pankreasa. Ključne faze razvoja embrionalnog pankreasa uključuju razvoj definitivne endoderme (DE), primitivne crijevne cijevi (PGT), pankreasa progenitora (PP), endokrinog progenitora (EP) i endokrinih ćelija koje eksprimiraju hormone. Dodavanjem različitih citokina (npr. epidermalni faktor rasta, bFGF) i modulatora signalizacije (npr. koštani morfogenetski proteini, inhibitori γ-sekretaze) u svaku fazu kako bi se aktivirali ili inhibirali specifični signalni putevi (npr. Notch, Wnt) uključeni u stvaranje odraslih β ćelija, sudbina hPSC ćelija se manipuliše u fenotip β ćelija.
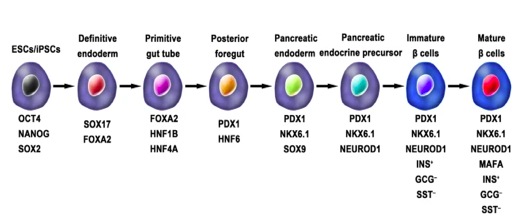
Slika 3. Diferencijacija β ćelija koje proizvode inzulin iz hPSC-a oponašanjem in vivo razvoja embrionalnog pankreasa
Istraživanje o liječenju dijabetesa tip 1 pomoću matičnih stem ćelija traje godinama i nastavit će se još dugo istraživati. Dva glavna izazova su pronalaženje adekvatne zalihe ćelija koje proizvode inzulin i zaštita ovih ćelija od napada imunološkog sistema. Postignut je impresivan napredak u rješavanju problema opskrbe beta ćelijama u smislu da je sada moguće generirati ćelije koje proizvode inzulin iz ljudskih ESC i iPS ćelija.
Nekoliko tipova ćelija pankreasa dobijenih iz matičnih ćelija je predloženo za transplantaciju u dijabetičke modele, uključujući progenitore pankreasa i ćelije koje luče insulin. Kako se endokrini progenitori razlikuju, migriraju kohezivno i formiraju prekursore otočića nalik pupoljcima. Sve veći broj dokaza ukazuje da pravilna regulacija glukoze zahtijeva koordinaciju između različitih tipova stanica otočića; stoga bi moglo biti korisno proizvesti čitava otočića in vitro umjesto diferenciranja ćelija u određeni tip.
Kada se kondicioniraju da sazriju in vivo, transplantirane progenitorne ćelije pankreasa proizvode ćelije koje luče inzulin koje sprječavaju ili poništavaju dijabetes nakon transplantacije. Prijavljeno je da transplantacija progenitora pankreasa dobijenih iz matičnih ćelija na skele koje oslobađaju eksendin-4 pospješuje usađivanje progenitora pankreasa iz matičnih ćelija i njihovo sazrijevanje prema β ćelijama koje proizvode inzulin, značajno povećavajući nivoe C-peptida i smanjujući glukozu u krvi u STZ -induciranim miševima. Hronična hiperglikemija i imunodeficijentno okruženje ubrzavaju sazrijevanje transplantiranih progenitornih ćelija ispod bubrežne kapsule kod miševa. Kontakt između ćelije progenitora pankreasa prije transplantacije je ključan za sazrijevanje u IPC in vivo. Ipak, in vivo sazrijevanje ostaje kritično pitanje koje treba riješiti. Očekuje se da će zrele endokrine ćelije stvorene in vitro brže preokrenuti dijabetes od progenitornih stanica pankreasa nakon transplantacije. Razvoj novih tehnika je neophodan za in vitro protokole diferencijacije koji mogu efikasno usmjeriti progenitorne ćelije dalje niz razvojni put β ćelija.
Za liječenje se koristi:
- Izrada beta ćelija od embrionalnih matičnih ćelija ili iPS ćelija. Embrionalne matične ćelije i iPS ćelije mogu se uzgajati u velikom broju u laboratoriji i imaju potencijal da budu natjerane da postanu bilo koji tip ćelija u tijelu, uključujući beta ćelije koje proizvode inzulin, uključujući senzore glukoze. Nedavni skokovi naprijed u ovim tehnologijama čine ovo vrlo obećavajućim putem za stvaranje velikog broja zamjenskih beta ćelija.
- Stimulišu beta ćelije da naprave mnogo više kopija sebe. Beta ćelije to mogu učiniti u pankreasu, ali obično vrlo sporo, a sve manje kako starimo. Istraživači traže lijekove koji bi mogli poboljšati samoobnavljanje kao mogući tretman za osobe s dijabetesom tipa 2 ili ranom stadijumom dijabetesa tipa 1.
- Zaštita beta ćelija od imunološkog napada: Imunolozi i bioinženjeri rade na nizu strategija za zaštitu transplantiranih ćelija od imunološkog napada. Jedan pristup je korištenje ćelijskog inženjeringa kako bi se stanice učinile otpornijima na takav napad, a drugi je inkapsuliranje ćelija unutar polupropusnih membrana kako bi se zaštitile od ćelija imunog sistema. Takve kapsule su porozne i omogućile bi malim molekulima kao što su glukoza i inzulin da prođu, štiteći beta ćelije od ćelija imunog sistema.
Ključ za ove pristupe je postavljanje beta ćelija na mjesto u tijelu gdje mogu raditi i zaštita od onoga što ih je prvo oštetilo. Ovo uključuje transplantaciju u dijelove tijela gdje je manja vjerovatnoća da će zamjenske ćelije biti napadnute od strane imunološkog sistema ili smještaj ćelija u zaštitne kapsule. Takve kapsule su porozne i omogućile bi malim molekulima kao što su glukoza i inzulin da prođu, štiteći beta ćelije od ćelija imunog sistema.
Pored stvaranja IPC iz obnovljivih matičnih ćelija, njihova imunomodulatorna, samoobnavljajuća i diferencijacijska svojstva također sugeriraju MSC kao potencijalno nove terapeutske kandidate u liječenju komplikacija povezanih s dijabetesom. Retinopatija, kritična ishemija ekstremiteta i nefropatija su najčešće i štetne komplikacije povezane s dijabetesom. Napredak u istraživanju matičnih ćelija pokazao je preokret ovih komplikacija kroz transplantaciju matičnih ćelija.
Potencijalni efekti liječenja dijabetesa stem ćelijama:
1. Liječenje hiperglikemije
2. Odgovor na test tolerancije glukoze
3. Dokaz odgovarajuće sekrecije C-peptida
4. Dobivanje na težini
5. Brzi povratak dijabetesa kada se uklone gen za transfekciju i/ili ćelije koje proizvode insulin
6. Nema regeneracije otočića životinja tretiranih stereptozotocinom i nema regeneracije pankreasa kod životinja s pankreatektomijom
7. Prisustvo granula za skladištenje insulina u tretiranim ćelijama
Prednosti stem ćelija
1. Pruža medicinske prednosti u oblastima terapijskog kloniranja i regenerativne medicine.
2. Pruža veliki potencijal za otkrivanje tretmana i izlječenja raznih bolesti uključujući Parkinsonovu bolest, šizofreniju, Alchajmerovu bolest, rak, ozljede kičmene moždine, dijabetes i mnoge druge.
3. Udovi i organi bi se mogli uzgajati u laboratoriji iz matičnih ćelija, a zatim koristiti u transplantaciji ili za pomoć u liječenju bolesti.
4. Pomoći će naučnicima da nauče o ljudskom rastu i razvoju ćelija.
5. Naučnici i doktori će moći da testiraju milione potencijalnih lijekova, bez upotrebe životinja ili ljudi. Ovo zahtijeva proces simulacije efekta koji lijek ima na određenu populaciju ćelija. Ovo će reći da li je lijek koristan ili ima bilo kakvih problema.
6. Istraživanje matičnih ćelija takođe koristi proučavanju razvojnih faza koje se ne mogu proučavati direktno u ljudskom embrionu, a koje su ponekad povezane sa velikim kliničkim posljedicama kao što su urođene mane, gubitak trudnoće i neplodnost. Sveobuhvatnije razumijevanje normalnog razvoja na kraju će omogućiti prevenciju ili liječenje abnormalnog ljudskog razvoja.
7. Prednost upotrebe odraslih matičnih ćelija za liječenje bolesti je da se vlastite ćelije pacijenta mogu koristiti za liječenje pacijenta. Rizici bi bili prilično smanjeni jer tijela pacijenata ne bi odbacila vlastite ćelije.
8. Embrionalne matične ćelije mogu se razviti u bilo koju vrstu ćelija u tijelu i tada mogu biti svestranije od matičnih ćelija odraslih.
Nedostaci
1. Upotreba embrionalnih matičnih ćelija za istraživanje uključuje uništavanje blastocista formiranih iz laboratorijski oplođenih ljudskih jajašaca. Za one ljude koji vjeruju da život počinje začećem, blastocista je ljudski život i uništavanje je nemoralno i neprihvatljivo.
2. Kao i svaka druga nova tehnologija, potpuno je nepoznato kakvi bi se dugoročni efekti takvog miješanja u prirodu mogli materijalizirati.
3. Embrionalne matične ćelije možda nisu rješenje za sve bolesti.
4. Nedostatak većine odraslih matičnih stanica je to što su one unaprijed specijalizirane, na primjer, krvne matične stanice stvaraju samo krv, a moždane matične stanice samo moždane stanice.
5. Oni su izvedeni iz embriona koji nisu pacijentovi i tijelo pacijenta ih može odbaciti.
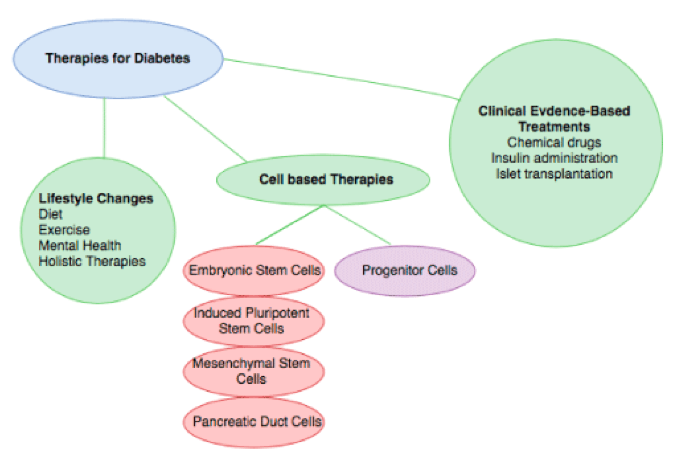
Slika 4. Terapije za liječenje dijabetesa, prirodnim putem i matičnim ćelijama
LITERATURA
https://hr.medicineh.com/28-stem-cell-therapy-cures-type-1-diabetes-in-mice-94238
https://stemcellres.biomedcentral.com/articles/10.1186/s13287-020-01793-6
https://www.sciencedaily.com/releases/2021/12/211202113432.htm
https://www.stetoskop.info/metode-u-medicini/lecenje-maticnim-celijama
https://hr.medicineh.com/96-stem-cells-may-treat-diabetes-48820