Ulkusna bolest želuca
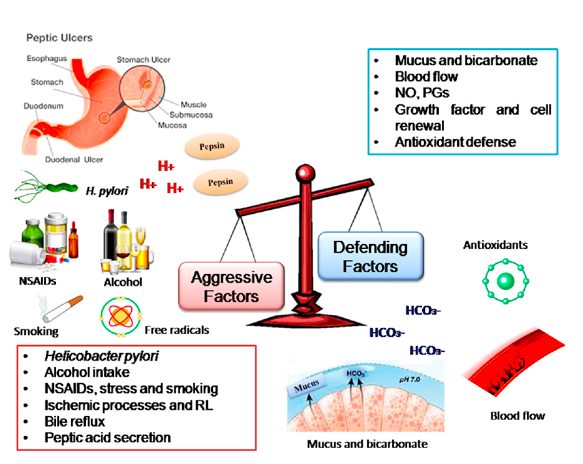
U razvoju gastričnog ulkusa ključni faktor je smanjenje otpornosti želučane sluznice na acido-peptično djelovanje želučanog soka, odnosno disbalans između protektivnih i agresivnih faktora. U smanjenju otpornosti želučane barijere važnu ulogu igra atrofični gastritis obzirom da atrofične promjene zahvataju sve vrste ćelijskih elemenata i to ćelije površnog sloja čija proliferativna uloga je bitan faktor u održanju mukozne barijere. Atrofične promjene zahvataju gastrične žlijezde, tako da se smanjuje i lučenje HCL-a i pepsina, kao i mukusne ćelije, te dolazi do smanjenog stvaranja mucina i surfaktanta i do nedovoljnog obnavljanja bikarbonata i pH gradijenta u sloju sluzi.
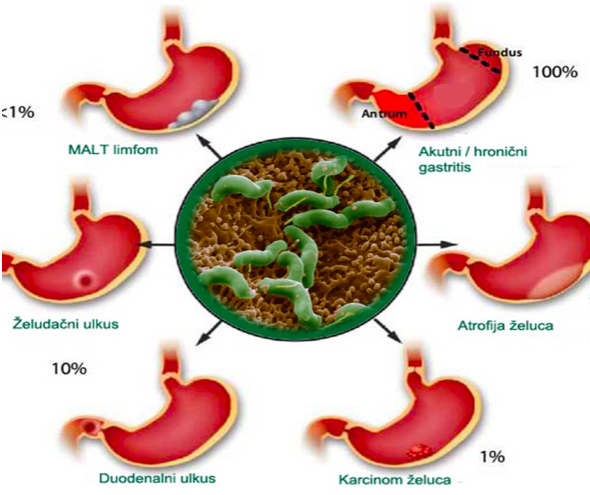
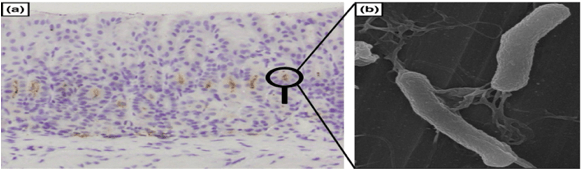
Kod 80% oboljelih od ulkusne bolesti želuca dokazana je infekcija sa Helicobacter Pylori. Naime, lipopolisaridi H.pylori sprječavaju vezivanje somatostatina za receptore čime se isključuje mehanizam inhibicije lučenja gastrina što uz istovremenu redukciju broja D-ćelija koje luče somatostatin, vodi povećanju nivoa gastrina sto često prati pojavu ulkusa. Do oštećenja sluznice sa povećanjem permeabilnosti dolazi zbog povećanog stvaranja slobodnih radikala koji nastaju djelovanjem neutrofila u toku inflamatorne reakcije, od kojih se H.Pylori štiti aktivnošću enzima superoksid-dismutaze, kao i razaranjem faktora rasta koji su neophodni za obnavljanje oštećene sluznice.
Pored infekcije sa H.Pylori svakodnevna upotreba NSAIL (Nesteroidni antiinflamatorni lijekovi), prvenstveno aspirina ali i ibuprofena, ketoprofena i drugih, povećava rizik od ravoja ulkusne bolesti za 10-20 puta. Dugotrajna upotreba NSAIL-a dovodi do submukozne erozije. Inhibicijom ciklooksigenaze NSAIL inhibiraju stvaranje citoprotektivnih prostaglandina i njihovih COX-2 udruženih efekat ( zaštita gastrične mukoze stimulacijom lučenja mukusa, bikarbonatne sekrecije, ćelijske proliferacije i povećanog protoka krvi).
Riziko faktori :
- Pušenje
- Stres
- Prezačinjena hrana,
- Alkohol i drugi.
U suštini, ovi faktori samostalno vjerovatno neće dovesti do ulkusa, ali mogu zakomplikovati samo stanje i otežati tretman istoga.
KLINIČKA SLIKA
Simptomi ulkusa želuca najčešće se javljaju u starijoj životnoj dobi sa najvećom incidencom u petoj dekadi. Najčešći simptom kod ulkusne bolesti želuca je epigastrična bol ili epigastrična nelagoda, no ona je manje tipična nego u pacijenata s duodenalnim ulkusom. U nekih pacijenata s ulkusom želuca bol nakon uzimanja hrane ne popušta. Nju zapravo hrana može izazvati ili pojačati, a smanjenje simptoma nakon primjene antacida nije tako postojano kao u pacijenata s duodenalnim ulkusom. Ulkusi želuca teže spontanom zarastanju, ali se i vraćaju, često na istome mjestu. Prepoznate epizode povrata aktivnosti ulkusa općenito se zapažaju rjeđe nego u duodenalnog ulkusa. Tačna učestalost ulkusa želuca nije poznata zato što je bolest u mnogih pacijenata s ulkusom želuca asimptomatska. Dok mučnina i povraćanje u pacijenata s duodenalnim ulkusom gotovo uvijek upućuju na opstrukciju želuca, u pacijenata s ulkusom želuca one mogu nastati i bez mehaničke opstrukcije. Gubitak tjelesne težine može nastati zbog anoreksije ili averzije prema hrani zbog neugodnosti izazvane njenim uzimanjem.
Krvarenje je česta komplikacija, a nastane u približno 25% slučajeva. Mortalitet je veći u pacijenata s ulkusom želuca nego u onih s ulkusom duodenuma. Perforacija želuca rjeđa je od krvarenja. Mortalitet uz perforaciju ulkusa želuca približno je tri puta veći nego uz perforaciju duodenuma. To je dijelom zbog veće životne dobi pacijenata s ulkusom želuca, ali također može biti i zbog nepostavljanja ili kasnog postavljanja dijagnoze ili zbog većeg onečišćenja peritoneuma uz perforaciju ulkusa želuca. Poremećaj pražnjenja zbog opstrukcije može nastati kada su ulkusi u piloričkom kanalu ili u najdistalnijem dijelu antruma, a vrlo rijetko uz druge lokalizacije u želucu.
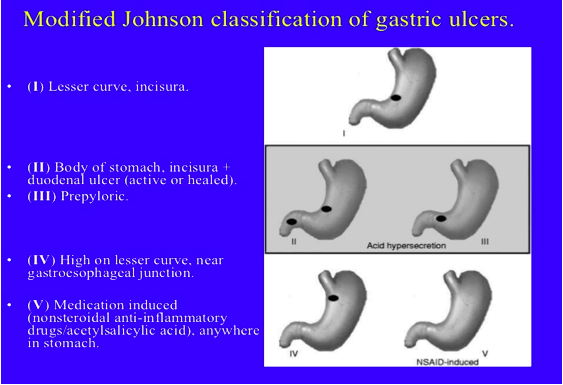
Johnson klasifikacija kliničkih tipova ulkusa želuca:
Tip I: predstavlja najčešći oblik i obično se javlja u želucu proksimalno od prepiloričnog antruma ili na incizuri male krivine ali bez zahvaćenosti duodenuma. Krvarenje se javlja rjeđe u odnosu na druge tipove. Nivo sekrecije HCL-a je obično nizak i ovaj tip se često javlja kod osoba krve grupe A.
Tip II: najčešče se javlja sekundarno, zbog otežanog pražnjenja kroz pilorus i simultanog duodenalnog ulkusa. Nivo sekrecije HCL-a je obično visok i ovakvi pacijenti često su prethodno imali duodenalni ulkus ili čak perforaciju ili kliničke znake gastrične opstrukcije. Često je prisutno noćno povraćanje i epigastrična bol. Ovi ulkusi imaju relativno lošu prognozu zbog rezistencije na medikamentoznu terapiju i skolonosti ka krvarenju. Preporučuje se hirurški tretman ukoliko ne postoje ozbiljnije kontraindikacije.
Tip III: u ovu skupinu pripadaju ulkusi koji su lokaliziranu u piloričnom kanalu ili prepiloričnoj regiji. Udruženi su sa acidnom hipersekrecijom te su slični duodenalnim ulkusima i češće se javljaju kod osoba sa krvnom grupom O.
Tip IV: ovdje pripadaju ulkusi koji su lokalizirani visoko na maloj krivini želuca blizu gastroezofagealnog sfinktera. Migracija neparietalne mukoze do nivoa ezofagogastričnog prijelaza je gotovo redovna tako da se ovaj tip smatra visokim tranzicionim varijetetom tipa I.
Tip V: može biti različite lokalizacije a posljedica je dejstva medikamenata.
KOMPLIKACIJE
Karcinom želuca: Pacijenti sa ulkusom čiji je nastanak vezan za infekciju H.Pylori imaju 3-6 puta veći rizik za razvoj karcinoma želuca, dok ulkusi druge etiologije ne nose povećan rizik za razvoj karcinoma.
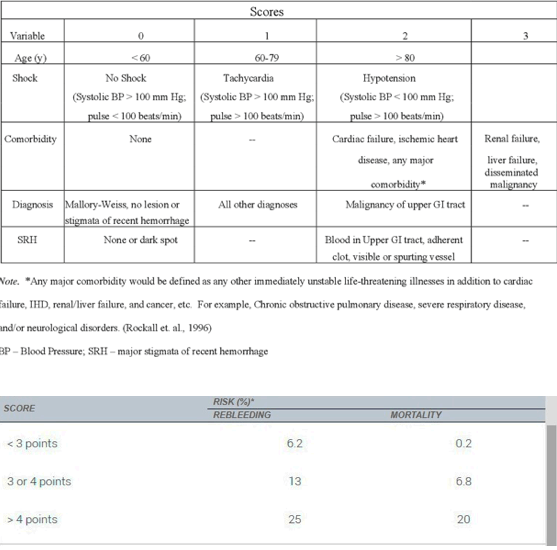
Krvarenje iz ulkusa želuca: je mnogo opasnije nego krvarenje iz ulkusa duodenuma, jer ima tendencu perzistentne hemoragije i teže se kontroliše. Krvarenje iz ulkusa zbog uzimanja NSAIL nastaje osobito često u nedostatku prethodnih ulkusnih simptoma. Uglavnom se manifestuje kod starijih pacijenata, kod kojih istovremeno postoje i drugi zdravstveni problemi. U većine pacijenata krvarenje iz peptičkog ulkusa zadovoljavajuće reaguje na medicinski tretman, uključujući gastričnu sukciju i IPP. Za procjenu rizika krvarenja kod pacijenata sa ulkusom koristi se Rockall score-system, na osnovu koga se mogu klasificirati pacijenti sa većim odnosno manjim rizikom od krvarenja.
Perforacija u peritonealnu šupljinu je praćena visokom stopom mortaliteta u poređenju sa perforacijom duodenalnog ulkusa, jer se perforacija češće javlja kod starijih osoba te se teže zbrinjava. Uz tipičnu pojavu iznenadnog bola u epigastrijumu, sa iradijacijom u lijevo rame ili bazu vrata, značajan je i nalaz pneumoperitoneuma. Prije perforacije 5-10% ovih pacijenata neće imati prepoznatljive simptome ulkusa. Obavezno se zabranjuje peroralni unos, u želudac se uvodi nazogastrična sonda za evakuaciju sadržaja, a parenteralno kristaloidni rastvori i antibiotici širokog spektra djelovanja.
Opstruktivni ulkus želuca je najčešći kod ulkusa tipa II i III. Opstrukcija se razvija dugotrajnim ožiljavanjem u antropiloričnoj regiji koje je praćeno značajnom inflamacijom neposredne okoline ulkusa. Simptomi su nadutost, mučnina, povraćanje i gubitak na tjelesnoj težini. Ovi pacijenti obično ulkusne simptome imaju mnogo godina, a često i simptome opstrukcije nekoliko mjeseci.
DIJAGNOZA
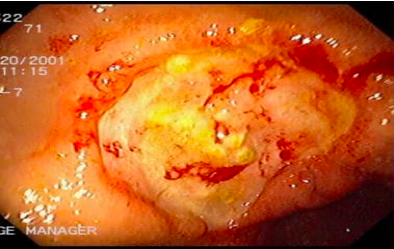
Endoskopija: Endoskopska vizualizacija ulkusa omogućava određivanje njegove veličine, lokalizacije, i nakon biopsije određivanje histoloških karakteristika. Predstavlja senzitivnu metodu u dijagnostici gastričnog ulkusa te omogućava uzimanje biopsije i citološku analizu u svrhu diferencijacije benignog od malignog stanja. Pored toga omogućava detekcije infekcije H.Pylori antralnom biopsijom i korištenjem brzog ureaza testa. U svrhu isključenja maligniteta na gastroskopiji je potrebno s unutarnjeg ruba i dna ulkusa uzeti najmanje 6 biopsija. Ako je dostupna precizna citološka dijagnostika prije biopsije treba četkicom ostrugati ulkus i uzeti uzorke. Indicirana je kod pod prisutnih dokaza krvarenja, gubitka tjelesne težine, hroničnog povraćanja, kod osoba koje ne reaguju na medikamentoznu terapiju (PPI), i osoba starijih od 55. godina sa prisutnim simptomima.
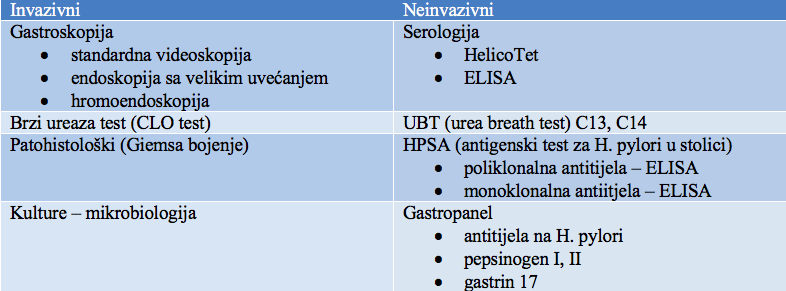
Dijagnostički testovi za H.Pylori :
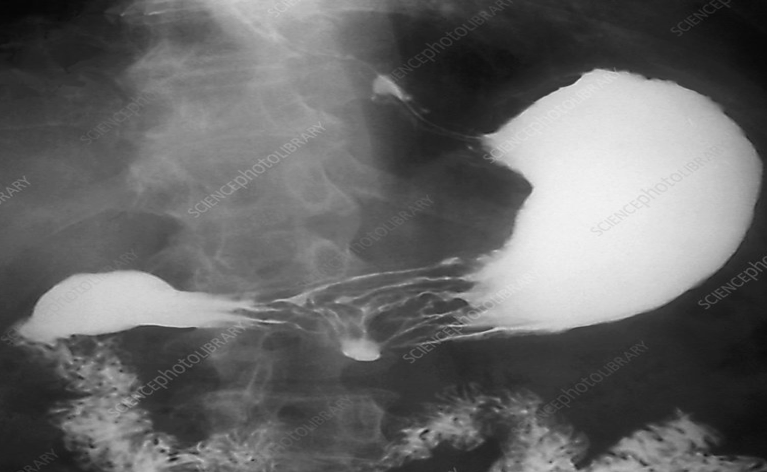
Radiografija: obično u ovu svrhu se koristi rendgenološko ispitivanje sa barijevom kašom ili gastrografinom (kontrastna radiografija) i to u prilikama kada nije moguća endoskopija ili kod sumnje na gastričnu opstrukciju, pri čemu je uspješnost dijagnostike preko 80 %. Pored toga radiografijom se može utvrditi prisustvo slobodnog vazduha kod sumnje na perforaciju ulkusa.
TERAPIJA
Terapija peptičnog ulkusa zavisi od njegove etiologije i kliničke manifestacije. Kod većine pacijenata je dovoljna eradikaciona terapija H.Pylori, prestanak uzimanja NSAIL i antisekretorna terapija(PPI). Prije svega, veoma bitno je otkloniti riziko-faktore koji dovode do razvoja ulkusa. Preporučuje se prestanak pušenja, prestanak konzumacije alkohola, izbjegavati uzimanje salilcilata i drugih NSAIL povezanih sa razvojem ulkusne bolesti, kao i kofeina obzirom da stimuliše sekreciju želučane kiseline.
Tretman krvarećeg ulkusa:
- Nepohodno je otvoriti 2 venska puta, odmah izvaditi KKS, koagulogram, ABS.
- Pacijent je nestabilan ukoliko je hipotenzivan, ubrzanog pulsa, preznojen i febrilan.
- Uljučuju se kristaloidi (2 litra odmah, te ako je i dalje hipotenzivan odmah trebovati transfuziju krvi),
- Nakon toga ordinirati 2 ampule pantoprazola (80 mg) u bolusu i ordinirati metoklorpramid intravenski.
- Nakon stabilizacije pacijenta, radi se urgentna endoskopija, tj. prvo restitucija pa tek onda endoskopija. Endoskopijom se može zaustaviti krvarenje korištenjem hemoklipsi, koagulacione terapije ili injekcije epinefrina.
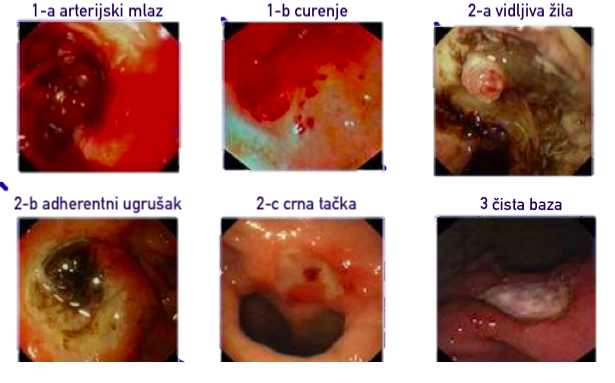
Forrestova klasifikacija krvarećeg ulkusa:
Tretman nekrvarećeg ulkusa:
- Pacijentu koji ne krvari i nema znakova komplikacija se preporučuje terapija IPP minimum 14-21 dan, a ukoliko je ulceracija veća, tretman može trajati i duži vremenski period.
- Ukoliko pacijent koristi ASA I NSAIL, onda se preporučuje da prekine istu terapije do cijeljenja, međutim ako pacijent koristi aspirin u cilju sekundarne prevencije inzulta, onda se on mora što prije vratiti terapiji, ali se preporučuje trajna gastroprotekcija, tj. sve dok troši aspirin, mora trošiti i IPP. Ukoliko je pacijent koristio NSAIL te se isti mora ponovo uključiti, preporučuje se probati zamijeniti lijek sa COX-2 inhibitorom uz IPP ili kontinuirana gastroprotekcija sa IPP uz NSAIL.
Terapija infekcije H.Pylori:
- koristi se trojna eradikaciona terapija koja podrazumjeva Amoksicillin kapsule 500 mg 2x2 u trajanju od 14 dana, Klaritromicin tablete 500 mg 2x1 ili Metronidazol tablete 500 mg 2x1 u trajanju od 14 dana i inhibitor protonske pumpe (pantoprazol tbl 20 mg 2x1 ili lansoprazol tbl 30 mg ili rabeprazol 20 mg 2x1 u trajanju od 7 dana, a nakon toga 1x1 u trajanju od 21 dan.)
- Kod alergije na penicilin, može se koristiti tetraciklin i metronidazol ili levofloxacin i metronidazol.
- Eradikaciju H.Pylori je najbolje pratiti antigen stool testom ili urea izdisajnim testom mjesec dana nakon prestanka terapije. Eradikacija se može pratiti i serološkim testovima ali nije pouzdana jer antitijela mogu biti pozitivna i do 3 godine nakon eradikacije, međutim ako je IgG manji za 30% u roku od pola godine od početka terapije, može se smatrati da je eradikacije uspješna.
Hirurško liječenje:
- Uz noviju farmakoterapiju značajno se smanjio i broj bolesnika kojima je potrebno hirurško liječenje i danas se rijetko provodi. Indikacije su perforacija, opstrukcija, nekontrolirano ili uporno krvarenje, sumnja na maligni želučani ulkus i simptomi refraktorni na farmakoterapiju.
- Hirurško liječenje se sastoji od postupaka za smanjenje lučenja kiseline kombiniranih s postupcima za omogućavanje pražnjenja želuca. Resekcijski hirurški postupci uključuju antrektomiju, hemigastrektomiju, parcijalnu gastrektomiju i suptotalnu gastrektomiju (odnosno resekciju 30 do 90% distalnog dijela želuca s gastroduodenostomijom—Billroth I ili gastrojejunostomijom—Billroth II) sa ili bez vagotomije.
- Pojava i vrsta postoperativnih simptoma razlikuje se ovisno o tipu operacije. Nakon resekcijskog zahvata do 30% bolesnika ima značajne simptome uključujući gubitak težine, lošu probavu, anemiju, tzv. dumping sindrom (sindrom brzog pražnjenja želuca + vazomotorni simptomi poslije obroka), reaktivnu hipoglikemiju, mehaničke probleme i recidiv ulkusa.
REFERENCE :
Ø https://www.mayoclinic.org/diseases-conditions/peptic-ulcer/symptoms-causes/syc-20354223
Ø Tai FWD, McAlindon ME. Non-steroidal anti-inflammatory drugs and the gastrointestinal tract. Clin Med (Lond). 2021;21(2):131-134. doi:10.7861/clinmed.2021-0039
Ø Gastric Ulcer: Classification, Blood Group Characteristics, Secretion Patterns and Pathogenesis H. DAINTREE JOHNSON, M.D., F.R.C.S. Postgraduate Medical School, London, England
Ø KALYANAKRISHNAN RAMAKRISHNAN, MD, FRCSE, and ROBERT C. SALINAS, MD, University of Oklahoma Health Sciences Center, Oklahoma City, Oklahoma Am Fam Physician. 2007 Oct 1;76(7):1005-1012.
Ø Huang JQ, Sridhar S, Hunt RH. Role ofHelicobacter pylori infection and non-steroidal anti-inflammatory drugs in pepticulcer disease: a meta-analysis. Lancet. 2002;359:14–22.
Ø Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson J, Loscalzo J. eds. Harrison's Principles of Internal Medicine, 18e. New York, NY: McGraw-Hill; 2012.
Ø Chey WD, Leontiadis GI, Howden CW, Moss SF. ACG Clinical Guideline: Treatment of Helicobacter pylori infection. Am J Gastroenterol. 2017 Feb. 112(2):212-39.
Ø Singh V, Mishra S, Maurya P, et al. Drug resistance pattern and clonality in H. pylori strains. J Infect Dev Ctries. 2009 Mar 1. 3(2):130-6.
Ø Cote GA, Howden CW. Potential adverse effects of proton pump inhibitors. Curr Gastroenterol Rep. 2008 Jun. 10(3):208-14.
Ø Stjepan Gamulin, Matko Marušić, Zdenko Kovač i suradnici, (2011): Patofiziologija, Medicinska naklada, ZAGREB, 2011.